Công thức tính phần trăm khối lượng và những bài tập tương quan là trong những chuyên đề trọng tâm của chương trình học lớp 10, 11. Công thức thành phần phần trăm theo khối lượng là gì? định hướng về bí quyết tính phần trăm khối lượng lớp 10?… vào nội dung bài viết chi tiết dưới đây, dnec.edu.vn sẽ reviews đến chúng ta các bí quyết tính phần trăm khối lượng, họ cùng tìm hiểu nhé !.
Mục lục
Công thức tính thành phần xác suất theo khối lượngCách tính phần trăm trọng lượng thường được sử dụngPhần trăm cân nặng là gì?
Phần trăm trọng lượng sẽ cho biết phần trăm của từng nguyên tố vào hợp chất hóa học.Để tìm xác suất khối lượng, chúng ta cần biết khối lượng mol của những nguyên tố trong hợp chất tính bằng gam / mol hoặc số gam của những chất tạo ra thành dung dịch.Phần trăm trọng lượng được tính bằng một công thức dễ dàng và đơn giản chia cân nặng của yếu tố (hoặc chất tan) cho cân nặng của hợp chất (hoặc dung dịch).Bạn đang xem: Công thức phần trăm khối lượng
Công thức tính thành phần tỷ lệ theo khối lượng
Công thức phần trăm trọng lượng hóa học
% A = ( frac m_ A m_ hh ). 100%
% B = ( frac m_ B m_ hh ). 100%
% C = ( frac m_ C m_ hh ). 100%
Bên trong:
(m_ hh = m_ A + m_ B + m_ C… )
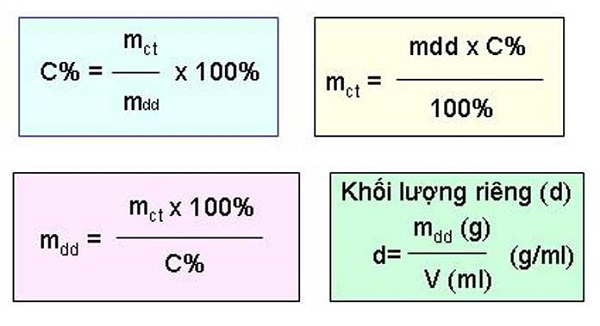
Công thức phần trăm cân nặng trong dung dịch
C% = ( frac m_ ct m_ dd ). 100%
(m_ ct = frac m_ dd 100 ). C%
(m_ dd ) = ( (m_ ct ). 100%): C%
Công thức tính tỷ trọng
(d = frac m_ dd V ) (g / ml)
Công thức về nồng độ mol / lít ( (C_ M ))
(C_ M = frac n V )
Bên trong:
n: số mol chất tan trong dung dịch (mol)V: thể tích hỗn hợp (lít)Công thức phần trăm theo thể tích (hoặc xác suất theo số mol)
Công thức phần trăm theo thể tích hoặc công thức tỷ lệ theo mol
% A = ( frac n_ A n_ hh ). 100%
Trong đó: (n_ hh = n_ A + n_ B + n_ C +… )
Công thức liên hệ giữa C%, (C_ M ) và tỷ lệ DỄ DÀNG
(C_ M = frac 10.D M ). C%
( Leftrightarrow ) C% = ( frac C_ M .M 10.D )
Cách tính phần trăm khối lượng thường được sử dụng
Tính phần trăm trọng lượng khi biết khối lượng
Bước 1: Tính cân nặng mol của hợp chất (A_ x B_ y )Bước 2: Tính số mol mỗi nguyên tố có trong một mol hợp chất (A_ x B_ y ). 1 mol phân tử (A_ x B_ y ) có: x mol nguyên tử A cùng y mol nguyên tử B.Tính khối lượng của những nguyên tố có trong một mol hợp hóa học (A_ x B_ y ). (m_ A = x.M_ A ) (m_ B = x.M_ B )Tính thành phần tỷ lệ theo khối lượng của từng nguyên tố theo công thức:% (m_ A ) = ( frac m_ A m_ A_ x B_ y ). 100%% (m_ B ) = ( frac m_ B m_ A_ x B_ y ). 100%Hoặc% (m_ B ) = 100% -% (m_ A )Tính phần trăm trọng lượng khi không biết khối lượng
Bước 1: khẳng định phương trình phần trăm cân nặng trong vừa lòng chất
Viết phương trình làm việc đầu bài: Phần trăm cân nặng = (phân tử khối của nhân tố / phân tử khối của thích hợp chất) x 100.Đơn vị của hai quý hiếm này là gam trên mol (g / mol).Khi bài xích toán không cho khối lượng, chúng ta cũng có thể dùng cân nặng mol nhằm tính phần trăm trọng lượng của nguyên tố.Bước 2: Viết công thức hóa học
Nếu đề bài bác không gửi ra công thức hóa học của từng hợp hóa học thì họ cần viết bọn chúng ra. Nếu câu hỏi về phương pháp hóa học tập thì bỏ qua mất bước này và gửi sang cách “Tìm cân nặng của từng nguyên tố”.Bước 3: Tìm cân nặng của từng thành phần trong phù hợp chất.
Tra trọng lượng phân tử của từng nguyên tố trong bí quyết hóa học tập trên bảng tuần hoàn. Cân nặng nguyên tố thường xuyên được viết dưới ký hiệu hóa học. Viết khối lượng của từng nhân tố trong vừa lòng chất.Bước 4: Nhân trọng lượng nguyên tử với tỉ lệ mol.
Xác định số mol (tỉ lệ mol) của mỗi nguyên tố trong hợp hóa học hoá học. Phần trăm mol được xem bằng số thấp rộng trong công thức hóa học của thích hợp chất. Nhân khối lượng nguyên tử của từng nguyên tố với tỉ trọng số mol.Bước 5: Tính tổng cân nặng của đúng theo chất.
Cộng khối lượng của toàn bộ các thành phần trong phù hợp chất.Tổng khối lượng của một hợp chất có thể được đo lường thông qua tỷ lệ mol. Con số này đang là chủng loại số trong phương trình xác suất khối lượng.Xem thêm: Stt Tâm Trạng Buồn, Những Câu Stt Tâm Trạng Nhất, Những Câu Status Buồn Và Tâm Trạng Nhất
Bước 6: Xác định khối lượng của nguyên tố để tính tỷ lệ khối lượng.
Khi việc yêu cầu các bạn tìm “phần trăm khối lượng”, bạn phải tìm khối lượng của một nguyên tố cụ thể trong một hợp hóa học dưới dạng xác suất của tổng khối lượng của toàn bộ các nguyên tố. Xác định và ghi trọng lượng của nguyên tố đó. Cân nặng này là cân nặng được biểu thị bằng phần trăm mol. Số lượng này là tử số trong phương trình tỷ lệ khối lượng.Bước 7: Thay những biến vào phương trình tỷ lệ khối lượng.
Sau khi khẳng định giá trị của từng biến, chỉ việc thay nó vào phương trình được khẳng định ở bước đầu tiên:
Phần trăm cân nặng = (khối lượng phân tử của yếu tố / cân nặng phân tử của thích hợp chất) x 100.
Bước 8: Tính phần trăm khối lượng.
Bây tiếng phương trình đã có điền vào, bạn chỉ việc tính phần trăm khối lượng.
Chia cân nặng của nguyên tố mang lại tổng trọng lượng của hợp chất rồi nhân cùng với 100. Đây là phần trăm khối lượng của yếu tố trong phù hợp chất.
Bài tập về công thức tính phần trăm cân nặng lớp 10
Bài 1: Oxi hóa hoàn toàn 0,135 gam hợp hóa học hữu cơ A rồi cho sản phẩm lần lượt đi qua bình 1 đựng chất rắn (H_ 2 SO_ 4 ) với bình 2 đựng KOH thì khối lượng bình 1 tạo thêm 0,117 gam. , bình 2 tăng 0,396 gam. Trong một phân tích khác, khi làm cho nóng 1,35 g hợp chất A với CuO thì nhận được 112 ml (dktc) khí nitơ. Tính thành phần tỷ lệ các nhân tố trong phân tử của hóa học A.
Dung dịch
Sự tăng thể tích của bình 1 là khối lượng của (H_ 2 O )
( Rightarrow n_ H = 2n_ H_ 2 O = frac 2.0,117 18 = 0,013 , mol )
Sự tăng thể tích của bình 2 là khối lượng của (CO_ 2 )
( Rightarrow n_ C = n_ CO_ 2 = frac 0,396 44 = 0,009 , mol )
Số mol của N bao gồm trong 0,135 gam hợp chất hữu cơ A là:
(n_ N = n_ N_ 2 = frac 2.0,112 22,4.10 = 0,001 , mol )
Vì thế:
% (m_ C ) = ( frac 12.0.009 0.135 ). 100% = 80%
% (m_ H ) = ( frac 1.0,0013 0,135 ). 100% = 9,63%
% (m_ N ) = ( frac 14.0.001 0.135 ). 100% = 10.37%
% (m_ O ) = 100% – (80% + 9,63% + 10,37%) = 0%
Bài 2: Oxi hóa trọn vẹn 0,6 gam hợp chất hữu cơ A thu được 0,672 lít khí (CO_ 2 ) (dktc) cùng 0,72 gam (H_ 2 O ). Tính thành phần phần trăm cân nặng của các nguyên tố trong phân tử của chất A?
Dung dịch
Oxi hóa A tạo thành (CO_ 2 ) và (H_ 2 O )
( Rightarrow ) Hợp hóa học A tất cả C, H có thể có O.
(n_ CO_ 2 = frac 0,672 22,4 = 0,03 , mol )
(n_ H_ 2 O = frac 0,72 18 = 0,04 , mol )
( Rightarrow n_ C = n_ CO_ 2 = 0,03 , mol )
(n_ H = 2n_ H_ 2 O = 0,08 , mol )
Vì thế:
% (m_ C ) = ( frac 12.0.03 0.6 ). 100% = 60%;
% (m_ H ) = ( frac 1,0,08 0,6 ). 100% = 13,33%
% (m_ O ) = 100% – (60% + 13,33%) = 26,67%
Như vậy, nội dung bài viết trên đây đã giúp ích cho chúng ta trong quy trình học về chủ thể công thức tỷ lệ khối lượng. Mong muốn những bí quyết tính phần trăm thể tích mà dnec.edu.vn sẽ tổng hợp để giúp đỡ ích cho chúng ta trong quá trình học tập. Chúc như ý với các nghiên cứu của bạn!.














